

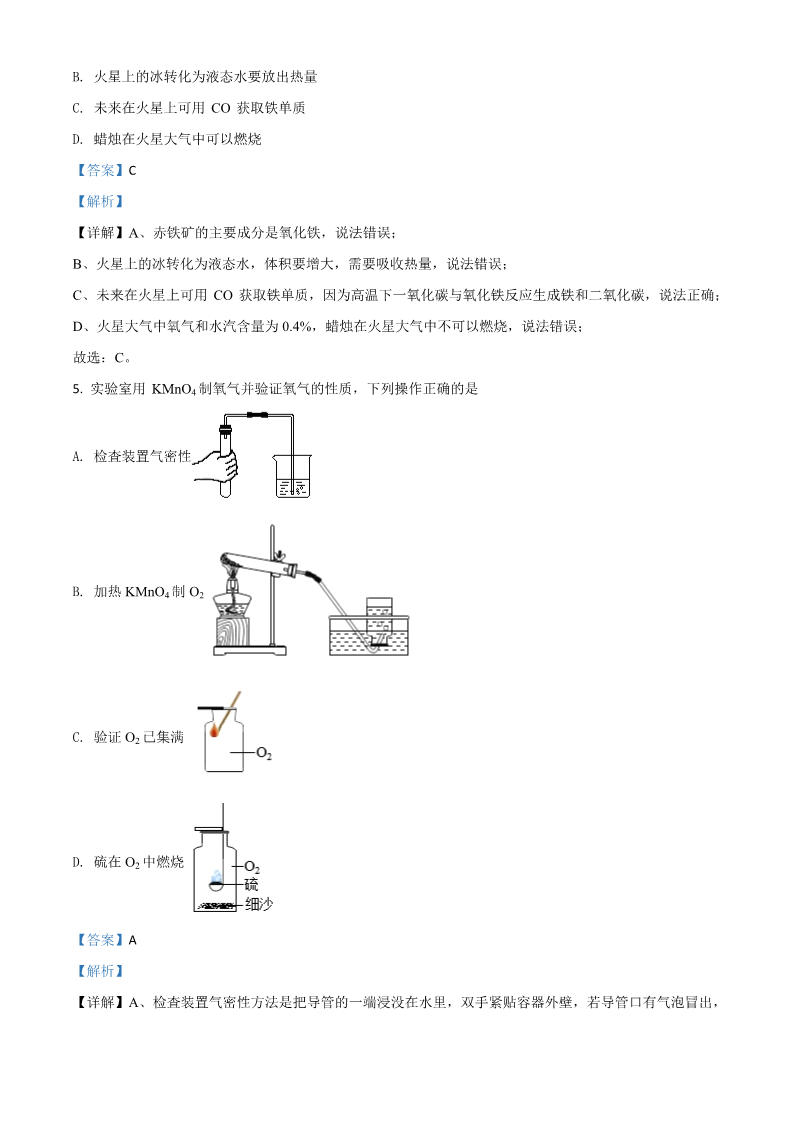


绵阳市 2020 年初中学业水平考试暨高中阶段学校招生考试 (化学部分) 可能用到的相对原子质量:H 1C 12N 14O 16Cl 35.5Na 23Mg 24Fe 56Ag 108 一、选择题(本题包括 9 小题,每小题 4 分,共 36 分。每小题只有一个选项最符合题目要 求) 1. 下列诗句或俗语中,涉及化学反应的是 吹尽黄沙始见金 A. B. 爝火燃回春浩浩 C. 酒香不怕巷子深 D. 铁杵磨成绣花针 B【答案】 【解析】 【分析】 化学变化是有新物质生成生成的变化。 【详解】A、吹尽黄沙始见金,没有新物质生成,属于物理变化,故 A 不正确; B、爝火燃回春浩浩,有新物质生成,属于化学变化,故 B 正确; C、酒香不怕巷子深是分子的运动,没有新物质生成,属于物理变化,故 C 不正确; D、铁杵磨成绣花针,没有新物质生成,属于物理变化,故 D 不正确。故选 B。 【点睛】物理变化是没有新物质生成的变化。 2. 2020 年 5 月 12 日是第十二个全国防灾减灾日,为预防森林火灾,应张贴的标志是 A. B. C. D. D【答案】 【解析】 AA【详解】 、该标志是循环利用标志。故不符合题意; BCB、该标志是有毒品的标志。故 不符合题意; C、该标志是节水标志。故 不符合题意; DD、该标志是禁止火种标志,为预防森林火灾,应该张贴该标志。故 符合题意。 D故选 。 3. “关爱生命,拥抱健康”是人类永恒的主题,下列说法科学的是 甲醛有防腐作用,但不能用于浸泡食材 A. B. 铁强化酱油因添加了铁单质可预防贫血病 C. 纤维素不能被人体消化,因此对人体健康无益 医用酒精用于防疫消毒,其中乙醇的质量分数为 75% D. A【答案】 【解析】 【详解】A、甲醛有毒,不能用于浸泡食材,符合题意; B、铁强化酱油因添加了铁元素可预防贫血病,不符合题意; C、纤维素能促进胃肠的蠕动,纤维素虽然不能被人体消化;但对人体也是有益的,不符合题意; D、医用酒精中乙醇的体积分数为 75%,不符合题意。故选 A。 4. 今年我国将发射火星探测器。以下是关于火星的部分已知信息: ①其橘红色外表是因为地表被赤铁矿覆盖; ②火星上无液态水,但有大量冰; ③火星大气的成分为二氧化碳 95.3%、氮气 2.7%、氩气 1.6%、氧气和水汽 0.4%。 下列说法正确的是 A. 赤铁矿的主要成分是四氧化三铁 B. 火星上的冰转化为液态水要放出热量 C. 未来在火星上可用 CO 获取铁单质 D. 蜡烛在火星大气中可以燃烧 C【答案】 【解析】 【详解】A、赤铁矿的主要成分是氧化铁,说法错误; B、火星上的冰转化为液态水,体积要增大,需要吸收热量,说法错误; C、未来在火星上可用 CO 获取铁单质,因为高温下一氧化碳与氧化铁反应生成铁和二氧化碳,说法正确; D、火星大气中氧气和水汽含量为 0.4%,蜡烛在火星大气中不可以燃烧,说法错误; 故选:C。 5. 实验室用 KMnO4 制氧气并验证氧气的性质,下列操作正确的是 A. 检査装置气密性 B. 加热 KMnO4 制 O2 C. 验证 O2 已集满 D. 硫在 O2 中燃烧 A【答案】 【解析】 【详解】A、检査装置气密性方法是把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出, 装置不漏气,故 A 正确; B、高锰酸钾是粉末状的,为防止高锰酸钾进入导管,要在试管口塞一团棉花,故 B 不正确; C、氧气的验满,带火星的木条要放在集气瓶口,木条复燃,说明已收集满,故 C 不正确; D、硫在氧气中点燃生成二氧化硫,二氧化硫和水反应,则硫在 O2 中燃烧集气瓶底部要加入水,故 D 不正 确。故选 A。 6. 我国科学家成功实现了用 CO2 和 CH4 合成醋酸,其反应的微观示意图如下。下列说法错误的是 A. 反应物、生成物均为有机物 B. 反应前后保持不变的粒子是原子 C. 醋酸可使紫色石蕊溶液变成红色 D. 反应前后催化剂的质量和化学性质无变化 A【答案】 【解析】 【分析】 催化剂 由该反应的微观过程可知,该反应的反应方程式为:CH4+CO2 C2H4O2; 【详解】A、有机物一般是指含碳的化合物,无机物一般是指不含碳的化合物,碳的氧化物、碳酸、碳酸盐 等性质与无机物相似,常归为无机物。该反应中反应物甲烷为有机物,二氧化碳为无机物,生成物中 C2H4O2 为有机物,符合题意; 的B、根据质量守恒定律,由反应 方程式可知,该化学反应前后原子的种类和个数不变,不符合题意; C、醋酸显酸性,可使紫色石蕊溶液变成红色,不符合题意; D、反应前后催化剂的质量和化学性质均不改变,不符合题意。故选 D。 7. 对下列事实的解释错误的是 选项 事实 解释 AB涂抹碱性溶液可减轻蚊虫叮咬的痛痒 碱性物质可中和蚊虫分泌的蚁酸 电池中的铅汞等会造成水体和土壤污染 废旧电池属于有害垃圾,不可随意丢弃 CD制糖工业中常用活性炭脱色制白糖 灯泡中充氮气以延长使用寿命 活性炭可与有色物质发生化学反应 氮气的化学性质不活泼,可作保护气 A. A B. B C. C D. D C【答案】 【解析】 【详解】A、蚊虫叮咬分泌出蚁酸,蚁酸和碱性物质反应,则涂抹碱性溶液可减轻蚊虫叮咬的痛痒,故 A 正确; B、电池中的铅汞等会造成水体和土壤污染,则废旧电池属于有害垃圾,不可随意丢弃,故 B 正确; C、活性炭具有吸附性,可以吸附色素和异味,则制糖工业中常用活性炭脱色制白糖,故 C 不正确; D、氮气常温下化学性质不活泼,可作保护气,则灯泡中充氮气以延长使用寿命,故 D 正确。故选 C。 8. 盐湖地区人们常采用“夏天晒盐,冬天捞碱”的方法来获取 NaCl 和 Na2CO3。结合溶解度曲线判断,下列 说法错误的是 A. NaCl 的溶解度随温度变化不大 的B. 44 ℃时 Na2CO3 饱和溶液 质量分数为50% 的C. “夏天晒盐” 原理是让湖水蒸发结晶得到 NaCl D. “冬天捞碱”的原理是让湖水降温结晶得到 Na2CO3 B【答案】 【解析】 【详解】A、从溶解度曲线图知道,NaCl 的溶解度随温度变化不大,不符合题意; 50g 100%33.3% B、44 ℃时,Na2CO3 的溶解度是 50g,则此时饱和溶液的质量分数为: ,符合 100g+50g 题意; C、“夏天晒盐”的原理是让湖水蒸发结晶得到 NaCl,因为氯化钠的溶解度随温度的变化,影响不大,所以 适合用蒸发结晶的方式,不符合题意; D、“冬天捞碱”的原理是让湖水降温结晶得到 Na2CO3,碳酸钠的溶解度在 40 ℃以下是随温度的降低,溶解 度降低,因为冬天温度低,所以降低温度能够得到碳酸钠的晶体,不符合题意。故选 B。 9. 钨是熔点最高的金属。工业上用黑钨矿(主要成分为钨酸亚铁)冶炼钨的主要反应有: Δ4FeWO +4Na CO +O4Na2WO4 +2Fe2O3 +4X ①4232Na WO +2HCl=H WO +2NaCl ②③2424ΔH WOWO3 +H2O 24ΔWO +3H W+3H2O ④32下列说法错误的是 A. FeWO4 中 W 的化合价为+6 B. 反应①中 X 的化学式为 CO2 C. ②、③反应前后所有元素的化合价均无变化 D. 上述 4 步反应分别涉及 4 种基本反应类型 D【答案】 【解析】 【详解】A、FeWO4 中已知铁元素的化合价为+2 价,氧元素的化合价为-2 价;设 FeWO4 中钨元素(W)的 化合价为 x,根据化合价的原则(在化合物中正、负化合价的代数和为零),则(+2)+x+4×(-2)=0,解得 x=+6,故钨元素(W)的化合价是+6 价,不符合题意; B、反应①中反应前有铁原子 4 个,碳原子 4 个,氧原子 30 个,钨原子 4 个,钠原子 8 个,反应后现有 4 个钠原子,4 个铁原子,4 个钨原子,8 个钠原子,22 个氧原子,剩余 4 个碳原子和 8 个氧原子,有个公因 数 4,剩余一个碳原子和两个氧原子, 为二氧化碳化学式,所以 X 为 CO2 碳;不符合题意; C、②是复分解反应,各元素的化合价不变,反应③反应前后氢元素的化合价是+1 价,氧元素的化合价是-2 H WO 价;设 4 中钨的化合价是 y,在化合物中正、负化合价的代数和为零,则(+1)×2+y+4×(-2)=0, 2WO 解得 y=+6;设 3 中钨的化合价是 z,在化合物中正、负化合价的代数和为零,则 z+3×(-2)=0,解得 z=+6;则所有元素的化合价均无变化,不符合题意; D、①不是基本反应类型,②是两种化合物相互交换成分生成两种新的化合物的复分解反应,③是一种物质 生成多种物质的分解反应,④是一种化合物和一种单质反应生成一种单质和一种化合物的置换反应,上述 4 步反应涉及 3 种基本反应类型,不符合题意。故选 D。 二、(本题包括 2 小题,共 29 分) 10. 2020 年 6 月 23 日,长征三号乙运载火箭将北斗三号最后一颗组网卫星成功送入预定轨道,我国北斗导 航地位将进一步提升。从化学视角回答下列问题: (1)卫星制造使用了黄金、钛合金,其中用作天线的是_______。使用黄金制作卫星的电子元件,利用了 金的什么化学性质?__________(填序号)。 A 光泽好 B 耐磨、易加工 C 容易导电 D 很难被氧化 (2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其 中 x=______。铝合金比纯铝具有的优势是___________(写出 1 条即可)。 (3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4 作氧化剂。偏二甲肼中 C、H、N 的质量比为___(填 最简整数比)。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一 种单质,这种单质的化学式为_________,两种氧化物中相对分子质量较大的是______。 N2 (6). (1). (2). (3). (4). (5). 6:2:7 【答案】 钛合金 CO2(或二氧化碳) 【解析】 D5硬度大、强度大、耐腐蚀等 (7). 【详解】(1)卫星制造使用了黄金、钛合金,其中用作天线的是钛合金,其硬度大。使用黄金制作卫星的 电子元件,利用了金的化学性质稳定,很难被氧化的性质; 故填:D。 (2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,原 子中质子数=核外电子数,其中 x=33-2-8-18=5。铝合金比纯铝具有的优势是硬度大、强度大、耐腐蚀等(写 出 1 条即可)。 (3)偏二甲肼(C2H8N2)中 C、H、N 的质量比为(12×2):(1×8):(14×2)=6:2:7。火箭发射时,燃料 与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,根据质量守恒定律,化 学反应前后,元素的种类不变,反应物中含 C、H、N、O,故生成物中也应含 C、H、N、O,故应是生成 N二氧化碳、水和氮气,则这种单质的化学式为 2 ,两种氧化物中相对分子质量较大的是 CO2(或二氧化 碳)。 11. 海水提取粗盐后的母液还可用来提取金属镁,其流程如下: 回答下列问题: (1)如在实验室进行操作 a,使用玻璃棒的目的是_____,沉淀 A 的化学式是________ 。 (2)用贝壳生产石灰乳,发生反应的化学方程式有:__________ 、 ________。 (3)由 MgCl2 溶液得到 MgCl2·6H2O 晶体,需要进行的实验操作有:__________、 _________、过滤、洗 涤。 (4)用 203 t MgCl2·6H2O 晶体最多能制备金属镁 ______________t。 高温 CaCO3 CaO CO2 CaO H2O Ca(OH)2 (4). (1). (2). Mg(OH)2 (3). 【答案】 引流 (5). (6). (7). 24 蒸发浓缩 冷却结晶 【解析】 【详解】(1)实验室进行操作 a 是过滤,使用玻璃棒的目的是引流;氯化镁和氢氧化钙反应生成氢氧化镁 和氯化钙,则沉淀 A 的化学式是 Mg(OH)2; (2)用贝壳生产石灰乳,先碳酸钙高温分解成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,发生反 高温 CaCO CaO CO CaO H2O Ca(OH)2 应的化学方程式: 、;32(3)由 MgCl2 溶液得到 MgCl2·6H2O 晶体,需要进行的实验操作有:蒸发浓缩、冷却结晶、过滤、洗涤; (4)设能制备金属镁质量为 x,根据质量守恒定律有: MgCl2 6H2O Mg 203 24 203t x203 203t ,解得 x=24t。 24 x三、(本题包括 2 小题,共 25 分) 12. 文宏同学利用“金属树”趣味实验来验证 Zn、Cu、Ag 三种金属的活动性顺序。 (1)为确保实验效果,CuCl2 溶液和 AgNO3 溶液需现配。配制 50 g质量分数为 12%的 CuCl2 溶液,应称 量____g CuCl2,加水时应选用_____mL 的量筒。除量筒外,配制溶液还需要的玻璃仪器有____。 (2)向两个放有宣纸的培养皿中分别滴入适量 CuCl2 溶液、AgNO3 溶液,再放入锌粒,一段时间后观察到 的实验现象如图。 ①形成“铜树”时发生反应的化学方程式是_________。 ②仅用“铜树”和“银树”实验尚不能验证________的金属活动性顺序,需补充一个实验来证明,应选用的药品 是___________(可供选择的药品有:锌粒、铜丝、银丝、稀盐酸、CuCl2 溶液、AgNO3 溶液)。 (1). (2). (3). 烧杯、玻璃棒、胶头滴管(未答胶头滴管不扣分) (4). 【答案】 6.0 50 (5). Zn CuCl2 ZnCl2 Cu (6). Cu、Ag(或铜、银) 铜丝、AgNO3 溶液 【解析】 的【详解】(1)配制 50 g质量分数为 12% CuCl2 溶液,应称量 50g×12%=6.0g CuCl2,加水 46mL ,量取 水时应选用 50mL 的量筒。除量筒外,配制溶液还需要的玻璃仪器有烧杯、玻璃棒、胶头滴管。 (2)①形成“铜树”时发生反应为锌与氯化铜反应生成氯化锌和铜,反应的化学方程式是 Zn CuCl ZnCl Cu 。22②仅用“铜树”和“银树”实验证明金属活动性:锌>银、锌>铜,尚不能验证 Cu、Ag(或铜、银)的金属活 动性顺序,需补充一个实验来证明,应选用的药品是铜丝、AgNO3 溶液,若铜能置换出银,则可知金属活 动性:铜>银。 【点睛】考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题 的关键。 13. 某化学兴趣小组利用“化学喷泉”设计了如下实验:20 ℃时,用 250 mL圆底烧瓶收集一瓶纯净的 CO2, 按下图组装装置。用注射器缓缓注入 3 mL NaOH溶液,轻轻振荡烧瓶,打开止水夹,玻璃导管尖嘴处很快 产生“喷泉”,与此同时,C、E 装置中发生连锁反应。回答下列问题: (1)图中仪器 X 的名称是_______。 (2)注入 NaOH 溶液后,烧瓶内发生反应的化学方程式是________。 (3)“连锁反应”后,C 试管中溶液的颜色变化为_________;E 试管中的现象为_____,反应的化学方程式 为________。 (4)实验结束后,同学们发现圆底烧瓶中溶液呈红色,由此认为烧瓶中一定还有 NaOH 剩余,你认为是否 正确?______,说明原因:_________。 2NaOH CO2 Na2CO3 H2O (1). (2). (3). (4). 出现 【答案】 锥形瓶 红色变浅或褪去 (5). CuSO4 +2NaOH=Cu(OH)2 +Na2SO4 (6). (7). 生成碳酸钠的水溶 蓝色絮状沉淀 不正确 液也呈碱性,也可使酚酞变红 【解析】 【分析】 氢氧化钠和二氧化碳生成碳酸钠和水,稀盐酸和氢氧化钠反应生成氯化钠和水,硫酸铜和氢氧化钠生成氢 氧化铜和硫酸钠。 【详解】(1)图中仪器 X 的名称是锥形瓶。 (2)注入 NaOH 溶液后,烧瓶内发生反应是氢氧化钠和二氧化碳生成碳酸钠和水,故反应的化学方程式是 2NaOH CO Na CO H O 。2232(3)“连锁反应”中,D 中稀盐酸倒吸进 C 中,稀盐酸和氢氧化钠反应生成氯化钠和水,当氢氧化钠部分反 应,溶液颜色变浅,当氢氧化钠完全反应,溶液颜色褪去,故 C 试管中溶液的颜色变化为红色变浅或褪去; E 试管中氢氧化钠和硫酸铜反应生成氢氧化铜沉淀,故 E 试管中的现象为出现蓝色絮状沉淀,反应是硫酸 CuSO +2NaOH=Cu(OH) +Na SO 铜和氢氧化钠生成氢氧化铜和硫酸钠,故反应的化学方程式为 。4422(4)碳酸钠和氢氧化钠均显碱性,能使酚酞溶液变红色,故烧瓶中一定还有 NaOH 剩余是不正确的,原因 是生成碳酸钠的水溶液也呈碱性,也可使酚酞变红。 【点睛】碳酸钠和氢氧化钠均显碱性,能使酚酞溶液变红色。 四、(本题包括 1 小题,共 10 分) 14. 某袋装食品的脱氧剂由活性炭、铁粉和食盐混合而成,三者质量比为 2∶2∶1。现用该脱氧剂进行实验, 回答下列问题: (1)将该脱氧剂加入盐酸中,发生反应的化学方程式为________________。 (2)打开失效的脱氧剂小袋,发现里面出现了红褐色物质,该物质的主要成分是________(填化学式)。 5.0g 未经使用的该脱氧剂最多能够吸收氧气_____ g。 (3)用电子秤称取 7.20g 完全失效后的脱氧剂放入烧杯中,加入足量稀硝酸,充分溶解后过滤,滤渣为黑 色粉末。向所得滤液中加入足量 AgNO3 溶液,充分反应产生的沉淀质量为 2.87g。列式计算该失效脱氧剂 中 NaCl 的质量分数_____(计算结果精确到 0.1%)。 Fe 2HCl FeCl H 【答案】(1) 22(2)Fe2O3(或 Fe2O3·xH2O);0.86 (3)16.3% 【解析】 【详解】(1)将该脱氧剂加入盐酸中,铁粉与稀盐酸反应生成氯化亚铁和氢气,发生反应的化学方程式为: Fe 2HCl FeCl H 。22(2)打开失效的脱氧剂小袋,发现里面出现了红褐色物质,该物质是铁粉吸收食品袋中的氧气和水分生成 的,该物质的主要成分是 Fe2O3(或 Fe2O3·xH2O)。因为该脱氧剂由活性炭、铁粉和食盐混合而成,三者质 25g 2g ,设 5.0 g未经使用的 量比为 2∶2∶1,所以 5.0g 未经使用的该脱氧剂中铁的质量为: 2 2 1 2Fe3O Fe2O3 112 2g 112 48 该脱氧剂最多能够吸收氧气质量为 x,则 ,则 ,x=0.86g。 48 x2g x(3)设:该失效脱氧剂中 NaCl 的质量为 y。 NaCl+AgNO3 = AgCl + NaNO3 58.5 143.5 2.87g y58.5 y143.5 2.87g y=1.17g 1.17g 7.20g 100% 16.3% 该失效脱氧剂中 NaCl 的质量分数为: 。答:该失效脱氧剂中 NaCl 的质量分数为 16.3%。 本试卷的题干 0635
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





