

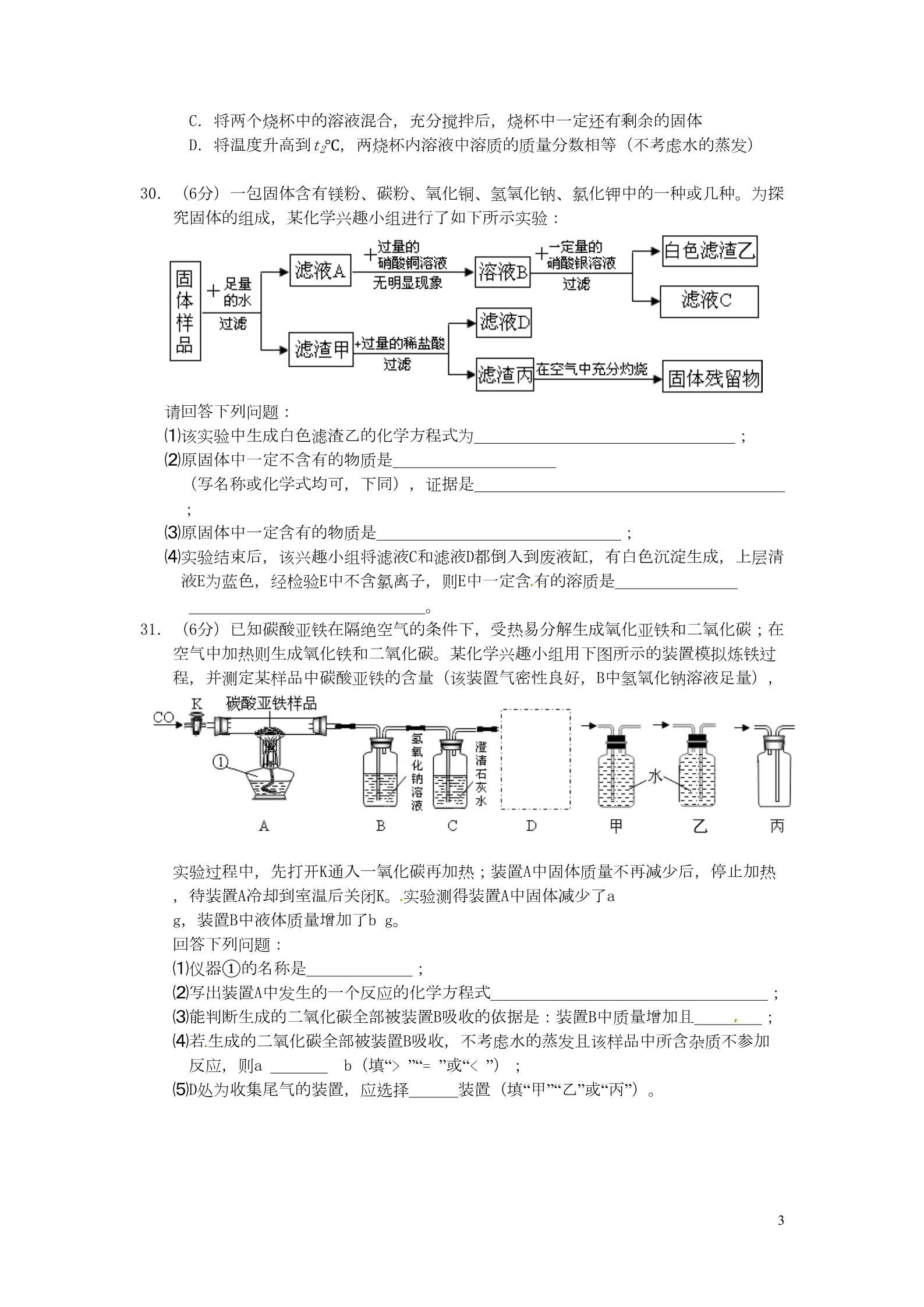


2016年武汉市中考化学试题 可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Fe-56 一、选择题(本题包括8小题,每小题只一个选项符合是题意,每小题3分,共24分) 1.下列变化不属于化学变化的是 A.粮食酿酒 B.盐酸除锈 C.冰雪融化 D.蜡烛燃烧 2.下列说法正确的是 A.墙内开花墙外香说明分子在不断运动 B.空气是由空气分子构成的 C.含有氧元素的化合物都是氧化物 D.不同元素最本质的区别是中子数不同 3.下列做法不正确的是 A.食用霉变的花生 B.合理摄入人体必需元素 C.使用可降解的塑料餐盒 D.用灼烧法鉴别合成纤维和羊毛纤维 4.生活中处处有化学。下列说法正确的是 A.纸张不可焕燃 B.乙醇汽油属于混合物 C.活性炭可将硬水软化 D.可用打火机检查天然气是否泄漏 点燃 5.某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O2==CO2+2H2O,下列关于X的 说法正确的是 A.X由碳、氢、氧三种元素组成 C.C中碳、氢元素的质量比为1:4 B.X的相对分子质量为10 D.X属于有机化合物 6.图1所示装置可用于测定空气中氧气的含量,其中与集气瓶相连的压强传感器等电子设 备能将集气瓶内压强精确地记录并保存下来。图2、图3是用该装置测得的红磷和木炭分 别在集气瓶中燃烧的压强-时间关系图(该装置气密性良好,P0是集气瓶内初始气压, P、P/分别是反应结束时恢复到室温时集气瓶内的气压) 下列说法正确的是 A.燃烧匙内所装红磷和木炭的多少对实验结果无影响 B.反应开始时集气瓶中压强瞬间变大是由燃烧放热造成的 C.P=0.79 P0,P/=P0是因为红磷的着火点比木炭低 D.由图3可推出空气中氧气的含量 7.甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系 如图所示。关于该转化关系图,下列说法正确的是 A.如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠 B.若甲、乙、丁都是氧化物,则丙一定是碳酸钙 C.甲、乙、丙、丁之间的转化可以全部通过复分解反应实现 1D.若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火, 则丙一定是单质碳 8.某粗盐样品除含有不溶性固体杂质我外,还含有少量的氯化镁、氯化钙,硫酸钠,某化 学兴趣小组开展如下探究活动: 探究一:除去粗盐中不溶性杂质 探究二:从滤液1中提取氯化钠固体(该探究中,微溶物不沉淀) 关于以上探究活动,有下列说法: ①试剂甲是碳酸钠溶液,试剂乙是氯化钡溶液 ②滤液1中的溶质一定有氯化钠,可能有氯化钙 ③若向探究二所得的白色滤渣中加入过量的稀盐酸,滤渣不溶解 ④往滤液4中加适量试剂丙时有中和反应发生 以上说法中正确的是 A.①③ B.①④ C.②③ D.②④ 二、非选择题(本题包括5小题,共26分) 28.(4分)氧元素的结构示意图如图所示。 ⑴该元素的原子核内质子数为 容易 电子(填“得到”或“失去”) ⑵由该元素组成的一种气体单质能供给呼吸,写出实验室制取该气体的一个化学方程 ;在化学反应中该原子 式。29.(4分)t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水两个烧杯中,充 分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。 ⑴烧杯②中的上层清液是否达到饱和状态? (填“是”、“否”或“无法判断”);⑵烧杯①中溶解的溶质是 (写名称或化学式); ⑶将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水 ⑷关于图1中烧杯内的物质,下列说法正确的是 g; 。A.烧杯①内溶液中溶质的质量分数 > 烧杯②内上层清液中溶质的质量分数 B.蒸发一定量的水,两烧杯中都一定有固体析出 2C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余的固体 D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发) 30.(6分)一包固体含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探 究固体的组成,某化学兴趣小组进行了如下所示实验: 请回答下列问题: ⑴该实验中生成白色滤渣乙的化学方程式为 ⑵原固体中一定不含有的物质是 (写名称或化学式均可,下同),证据是 ;;⑶原固体中一定含有的物质是 ;⑷实验结束后,该兴趣小组将滤液C和滤液D都倒入到废液缸,有白色沉淀生成,上层清 液E为蓝色,经检验E中不含氯离子,则E中一定含有的溶质是 。31.(6分)已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳;在 空气中加热则生成氧化铁和二氧化碳。某化学兴趣小组用下图所示的装置模拟炼铁过 程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量), 实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热 ,待装置A冷却到室温后关闭K。实验测得装置A中固体减少了a g,装置B中液体质量增加了b g。 回答下列问题: ⑴仪器①的名称是 ;⑵写出装置A中发生的一个反应的化学方程式 ;⑶能判断生成的二氧化碳全部被装置B吸收的依据是:装置B中质量增加且 ;⑷若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加 反应,则a b(填“﹥”“﹦”或“﹤”); ⑸D处为收集尾气的装置,应选择 装置(填“甲”“乙”或“丙”)。 332.(6分)某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下: Ⅰ.取一片胃药研碎,加水完全溶解得100g溶液; Ⅱ.配制100g 0.365%的稀盐酸作为模拟胃酸; Ⅲ.取上述一种溶液20g于锥形瓶中,再将另一种 溶液逐滴加入锥形瓶内,反应后溶液的pH变化 情况如图所示。 请回答下列问题 ⑴碳酸氢钠属于 (填“酸”“碱”或“盐”); ⑵步骤Ⅲ中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应(胃药中其它 成份不参加反应)。请依据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的 计算过程。 4武汉化学参考答案 一、选择题 题号 1C2A3A4B5D6B7C8D答案 二、非选择题 28.⑴8 得到 MnO2 ⑵2H2O2===== 2H2O+O2↑ (或2KMnO4====== K2MnO4 + MnO2 + O2↑ 和 2KClO3===2KCl+3O2↑ 中的任一个) 29. ⑴是 ⑵氯化钾 (或KCl)⑶50 ⑷AD 30. ⑴KCl+AgNO3=AgCl↓+KNO3 ⑵氢氧化钠 向滤液A中加过量的硝酸铜溶液无明显现象 MnO2 ⑶镁 氧化铜 氯化钾 ⑷硝酸铜 硝酸镁 硝酸钾 硝酸 31. ⑴酒精灯 高温 ⑵FeCO3====FeO+CO2↑(或FeO+CO==Fe+ CO2 ) ⑶装置C中的澄清石灰水没有变浑浊 ⑷﹤ ⑸乙 32. ⑴盐 ⑵分析可知滴入到锥形瓶的溶液为稀盐酸 参加加反应HCl的质量=10g×0.365%=0.0365g 设参加反应碳酸氢钠的质量为X NaHCO3 + HCl ===NaCl + H2O + CO2↑ 84 X36.5 0.0365g 84:X=36.5:0.0365g X=0.084g 每片胃药中碳酸氢钠的质量=0.084g×100g/20g=0.42g 答:略 5
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





