


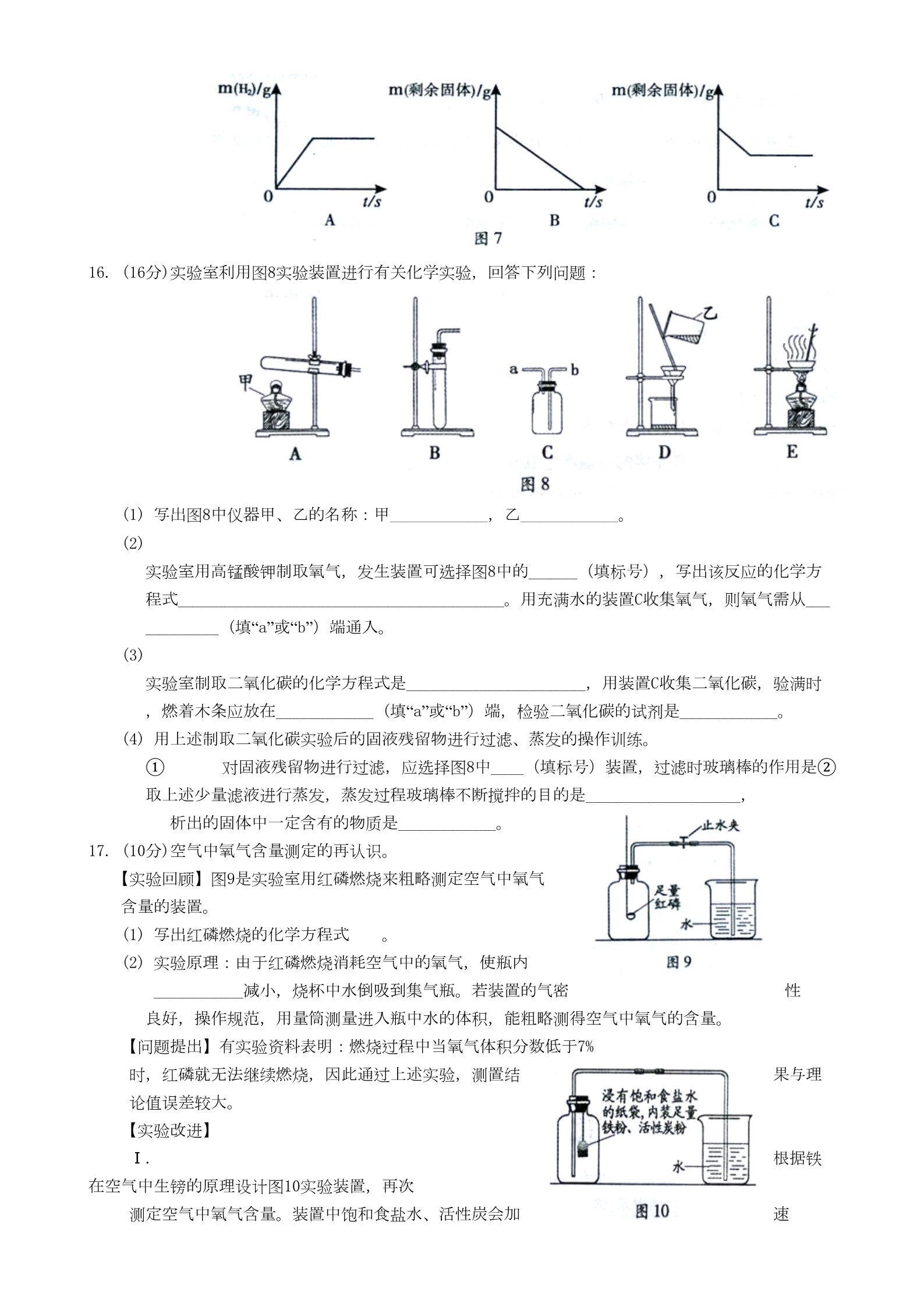

福建省福州市2015年中考化学真题试题 (全卷共6页,18题;满分100分;考试时间60分钟) 友情提示:请把所有答案填写(涂)在答题卡上,请不要错位、越界答题! 毕业学校_____________ 姓名_____________ 考生号_____________ 可能用到的相对原子质量:H – lC – 12N – 14O – 16Na – 23Ca – 40 第I卷 选择题(共36分) 第I卷包含12题,每题3分,共36分。每题只有一个选项符合题目要求,请在答题卡选择题栏内用2B 铅笔将正确选项涂黑。 1. 下列有关“化学与生活”的认识不科学的是 A. 天然气是应用广泛的燃料 B. 吃水果和蔬菜可以补充维生素 C. 可以食用甲醛溶液浸泡的海产品 D. 可降解塑料的问世减少了白色污染 2. 二氧化钛(TiO2)可作水分解的光催化剂,其中氧元素为 -2价,则钛元素的化合价为 A. +1 B. +2 C. +3 D. +4 3. 根据图1的信息判断,下列关于铝的说法错误的是 A. 属于金属元素 B. 原子的核电荷数是13 C. 相对原子质量是26. 982 g D. 在化学反应中,原子易失去电子形成Al3+ 4. 下列化学用语与含义不相符的是 A. O2- — 氧离子 B. 3H — 3个氢元素 C. Fe3O4 — 四氧化三铁 D. 2N2 — 2个氮气分子 5. 实验结束后,图2中仪器的处理方式正确的是 6. 市场上有“加碘食盐”、“高钙牛奶”、“含氟牙裔”等商品,这里的“碘、钙、氟”指的是 A. 单质 B. 元素 C. 分子 D. 原子 7. 下列关于水的说法正确的是 A. 所有物质都易溶于水 B. 可将工业废水任意排入内河 C. 生活中常用肥皂水检验软水和硬水 D. 水电解过程与电源正极连接的一端产生氢气 8. 几种常见物质的pH范围如表1,其中酸性最强的是 物质 酸奶 鸡蛋清 7 ~ 8 表1 牙育 肥皂水 pH范围(常温) 4 ~ 5 8 ~ 9 10 ~ 11 A. 酸奶 B. 鸡蛋清 C. 牙育 D. 肥皂水 9. 图3是某物质的分子模型,下列关于该物质说法正确的是 A. 属于有机物 B. 化学式为NH3 C. 氮元素和氢元素的质量比为3 :1 D. 氢元素的质量分数 10. 下列应用与中和反应原理无关的是 A. 用浓硫酸干燥湿润的氧气 B. 用熟石灰改良酸性土壤 C. 服用含氢氧化铝的药物治疗胃酸过多 D. 用氢氧化钠溶液洗涤石油产品中的残留硫酸 11. 下列鉴别物质所用的方法或试剂,错误的是 A. 氧气和氮气——观察颜色 B. 铁粉和炭粉——用稀硫酸 D. 氢氧化钠溶液和水——用酚酞溶液 C. 羊毛和化学纤维一-点燃闻气味 12. 实验室用硝酸钾固体配制100.0 g溶质质量分数为3.0%的硝酸钾溶液,下列说法正确的是 A. 用50mL量筒量水 B. 将固体放于托盘天平的右盘称取 C. 将固体直接投人童筒中溶解 D. 将配好的溶液装人贴有标签(如图4)的试剂瓶中,塞好瓶塞 第Ⅱ卷 非选择题(共64分) 13. (14分)多角度认识物质的变化,有助于我们更好地理解化学知识。 (1) 从微观角度 (图5为某化学反应的微观示意图,据图回答下列问题。) ① 微观上看,该化学变化中发生根本改变的微粒是____________(填“原子”或“分子”), 变化过程中,同种原子的个数____________ (填“有”或“没有”)增减。 ② 参加反应的A2与B2两种物质的分子个数比为 。 (2) 从反应类型角度 (一种物质可通过不同的反应类型生成,以二氧化碳为例。) ① 能与氧气化合生成二氧化碳的物质是____________(填一种物质化学式)。 ② 高温下,石灰石分解生成二氧化碳的化学方程式是________________________。 ③ 在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和________(填化学式)。 (3) 从能量变化角度 (借用图6装置分别进行下列实验,认识物质变化中的能量变化) ① 往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件 分析,此时生石灰的作用是__________________________。 写出生石灰与水反应的化学方程式____________________。 ② 将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷 燃烧的是_____________ (填标号)。 A. 氣化纳 B. 硝酸铵 C. 浓硫酸 D. 氢氧化钠 14. (10分)“比较归纳法”是学习化学的一种重要方法。(“―”表示相连的两种物质能发生反应,“→”表示 某种物质可通过一步反应转化为另一种物质。) (1) 请以表2中序号Ⅰ为示例,填写序号 Ⅱ、Ⅲ 中的空格: (2) 室温下,氯化镁与下列物质的变化关系,正确的是____________(填标号)。 A. MgCl2 — AgNO3 C. MgCl2 — HCl B. KNO3 — MgCl2 D. Mg(OH)2 — MgCl2 15. (10分)分析处理图表中的信息是学习化学的一种重要方法。 (1) 表3是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答: ①40℃时,氯化钠的溶解度为____________g。 ② 碳酸钠的溶解度随温度的升高而____________(填“增大”或“减小”)。在20℃时, 将100g的水加入30 g碳酸钠中,充分搅拌后得到的是____________(填“饱和溶液”或“不饱和溶液”),将上述溶液 升温到30$,该溶液的溶质质量分数为____________ (计算结果精确到0.1%)。 ③ 10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是______。 (2) 将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式_________________ _______。图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的 是____________(填标号)。 16. (16分)实验室利用图8实验装置进行有关化学实验,回答下列问题: (1) 写出图8中仪器甲、乙的名称:甲____________,乙____________。 (2) 实验室用高锰酸钾制取氧气,发生装置可选择图8中的______(填标号),写出该反应的化学方 程式________________________________________。用充满水的装置C收集氧气,则氧气需从___ _________ (填“a”或“b”)端通入。 (3) 实验室制取二氧化碳的化学方程式是______________________,用装置C收集二氧化碳,验满时 ,燃着木条应放在____________ (填“a”或“b”)端,检验二氧化碳的试剂是____________。 (4) 用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练。 ①对固液残留物进行过滤,应选择图8中____(填标号)装置,过滤时玻璃棒的作用是② 取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的目的是___________________, 析出的固体中一定含有的物质是____________。 17. (10分)空气中氧气含量测定的再认识。 【实验回顾】图9是实验室用红磷燃烧来粗略测定空气中氧气 含量的装置。 (1) 写出红磷燃烧的化学方程式 。(2) 实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内 ___________减小,烧杯中水倒吸到集气瓶。若装置的气密 良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。 【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结 论值误差较大。 性果与理 【实验改进】 Ⅰ. 根据铁 在空气中生镑的原理设计图10实验装置,再次 测定空气中氧气含量。装置中饱和食盐水、活性炭会加 速铁生锈。 Ⅱ.测得实验数据如表4 【交流表达】 (1) 铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2], 写出该反应的化学方程式_________________________________________。 (2) 根据表4数据计算,改进实验后测得的空气中氧气的体积分数是___________(计算结果 精确到0.1%)。 (3) 从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是: ①____________________________________________________; ②____________________________________________________。 18. (4分)某碳酸钠样品中混有少量氯化钠,根据图11所示信息计算该样品中碳酸钠的质量分数。(计算结 果精确到0.1%) (反应的化学方程式:CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl) 2015年福州市初中毕业会考、高级中等学校招生考试 化学试卷参考答案 第I卷选择题(包含12题。每题3分,共36分) 题号 1C2D3C4B5C6B7C8A9B10 A11 A12 D答案 第II卷非选择题(包含6题,共64分) 13. (14 分) ⑴ ① 分子没有 ⑵ ① C (合理均可) ② CaCO3 高温 CaO + CO2↑ ③ Fe ⑶ ① 生石灰与水反应放出大量热,水温升高,使温度达到白磷的着火点 CaO + H2O = Ca(OH)2 ② C ② 1:1 D14. (10分) ⑴ ① H2SO4 + BaCl2 = 2HCl + BaSO4↓ ② 新酸(合理均可) ③ CuSO4 + 2NaOH = CuSO4 + Cu(OH)2↓(合理均可) ④ 盐 ⑵ A D 15. (10 分) ⑴ ① 36.6 ② 增大 饱和溶液 23.1% ③ 碳酸钠饱和溶液 ⑵ Fe + 2HCl = FeCl2+H2↑ 16. (16 分) A C ⑴ 酒精灯 烧杯 ⑵ A 2KMnO4△ K2MnO4 + MnO2 + O2↑ aa⑶ CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ ⑷ ① D 引流 澄清石灰水 ② 使液体受热均匀、防止液体因局部过热而飞溅 氯化钙 17. (10 分) 【实验回顾】⑴ 4P + 5O2 点燃 2P2O5 ⑵ 气压 ⑵ 20.2% 【交流表达】⑴ 2Fe + 2H2O + O2 = 2Fe(OH)2 ⑶ ① 铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确。 ② 测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确。 18. (4 分) 解:设该样品中碳酸钠的质为x CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl 106 x100 5.0g x = 5.3g 样品中碳酸钠的质量分数 答:该样品中碳酸钠的质量分数为70.7%
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





